信使核糖核酸 (mRNA):激活免疫系统的漂流瓶
这简直是天方夜谭:我的身体可以借助新型信使核糖核酸(mRNA)疫苗生成自身的疫苗,在自己体内靶向击退有害病毒。这其中的奥秘在于通过“一个信息瓶 ”将特定蛋白质的图谱发送至人体内的细胞中,从而训练人体免疫系统开始与入侵身体的不速之客战斗。长期以来这项技术一直未得到重视,人们低估了它的潜力。如今, mRNA在医学研究领域前途不可限量,根据针对 COVID-19 的医学研究,它可能很快就能应用于预防癌症、疟疾和艾滋病。
文章概况:作为关键参与者,肖特医药确保 mRNA 疫苗的安全封装和交付,支持抗击癌症、疟疾和艾滋病毒等疾病的医学研究取得突破。
- mRNA 技术有望为个性化医疗和癌症和基因治疗研究中的创新疗法带来希望。
- mRNA 疫苗可以训练免疫系统对抗特定的病毒。
- 肖特医药为 mRNA 疫苗提供安全的封装和交付解决方案,确保它们安全送达患者。
人体如何精准定位,智慧地战胜病毒
目前的困境是:病毒不断变异。它们不断适应,更多新变种病毒不断成为主导。原疫苗越可靠,意味着对变异病毒疾病的有效性会降低,无法提供足够保护。特别在传染病大流行病期间,当全球许多人感染一种新病毒时,人类就要面临一个难题:传统疫苗研发和生产的周期太漫长了。
基于基因的技术可刺激人体自身产生疫苗,这为疫苗的研制开辟了新思路:mRNA可以直接将蛋白质图谱送入细胞,无需使用完整的病毒,也无需花费大量时间在实验室培养大量病原体或使用病原体抗原。这项技术无需活病毒或细胞培养,因此生产速度更快。mRNA可以直接合成,这极大提升了生产速度。然后,细胞利用图谱生产出与病毒表面蛋白质相似的特定蛋白质。免疫系统经过训练后会“记住”这些蛋白质,并在病毒进入人体后对其进行识别和打击。
早在新冠疫情之前,人们就已经开始研究mRNA 技术,用于治疗新型冠状病毒(COVID-19) 以外的疾病。为人体提供信息,帮助其决定制造何种特定的蛋白质,这为药物研发带来无限可能,并可能从根本上改变医药学。因为几乎所有疾病都是由错误蛋白质引起的。而mRNA 就如同烧红的刀枪剑戟,是对抗自身免疫性疾病、艾滋病和治疗癌症的利器。
疫苗的诞生
几个世纪以来,人类一直在寻求有效预防传染病的方法。1796 年,英国医生爱德华·詹纳(Edward Jenner)让一个小男孩感染了牛痘,然后孩子对天花产生了免疫力。人类终于找到了有效的方法,治疗这个可谓欧洲最危险疾病之一的传染病。
如今,疫苗仍在不断发展,其有效性也持续提高。更多人通过接种疫苗对狂犬病、白喉、流感、脊髓灰质炎和破伤风等疾病产生了免疫。1980 年,世界卫生组织(WHO)宣布天花已经灭绝。这是人类前所未有的成功。

mRNA 如何安全到达目标?
告诉细胞开始制造蛋白质是一项复杂的任务。那么如何才能将遗传密码成功送入细胞?
长期以来,这被认为是不可完成的任务。例如,mRNA 在细胞外时具有不稳定性,阻碍了细胞间的交换。这是一种预防基因误传的机制。同样,在哺乳动物体内,病毒的mRNA 会导致严重的炎症——因为免疫系统会将基因信息(就像病毒和细菌一样)识别为外来信息,并开启对抗。这意味着,只要信息没有保护机制,mRNA 就不适用于调节人体的免疫系统。

这催生了卡塔琳·卡里科(Katalin Karikó)和德鲁·魏斯曼(Drew Weissman)的研究成果。2005 年,两人找到了炎症反应的解决方案: 可能由于遗传密码的细微差异,哺乳动物的mRNA 不会像病毒的直接信息那样受到人体的直接对抗。研究人员循序渐进,修改了mRNA ,直到免疫系统无法识别它们。为此,他们使用脂质纳米颗粒(LNPs)作为递送材料。这些脂质颗粒环绕并保护着mRNA ,此时的mRNA 犹如一封放入漂流瓶的信件,即使在水上漂流也不会被浸湿。这为进入细胞铺平了道路——理论上,mRNA 现在已经可以用于治疗。
尽管mRNA 疫苗的有效性已经得到证实,在生产、运输和储存这几个环节仍然面临多个挑战。
mRNA 疫苗的研发从计算机演算开始,科学家借助计算机来确定将哪些遗传信息送入细胞。合成DNA,使用RNA 聚合酶来生成mRNA 单链。它们包含着重要的信息,例如被冠状病毒用来攻击人体细胞的刺突蛋白的基因序列。
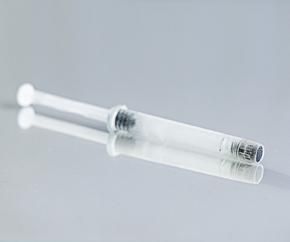
为确保mRNA 在送达患者时仍保有稳定性,必须将它储存于特定的医药包装内,并保存于0°C至 -100°C 的温度环境下。mRNA的运输通常依靠干冰箱,以此来保证恒定的低温运输环境。如果要将多剂量的活性成分装入注射剂瓶,并把它们安全运送至疫苗接种中心、手术地或医院,使用干冷链运输是理想的选择。当疫苗到达接种点后,可以将注射剂瓶从干冰箱中取出,放入普通冰箱存放数天。由于疫情期间的疫苗需求量极大,这是一个高效的运输系统。
随着感染人数减少,对疫苗的需求降低,疫苗剂型也从多剂量瓶转向了单剂量瓶。未来的研究应用将更偏向小批量的mRNA 药剂,即个性化医疗。这对包装和运输解决方案提出了新的要求。
革命性的研究
上图两位研究人员分别是生物化学家卡塔琳·卡里科(Katalin Karikó)和免疫学家德鲁·魏斯曼(Drew Weissman)。1997 年,他们偶然地在宾夕法尼亚大学内的一台复印机(!)前相遇。卡里科(Katalin Karikó)研究mRNA多年,刚开始她还只是一名匈牙利科学院的博士生。失业后,她远赴美国,继续研究mRNA。当时,魏斯曼(Weissman)正寻求研发一款抗艾滋病毒的疫苗,他注意到了卡塔琳·卡里科(Katalin Karikó)在这个领域的潜力。

在低温条件下mRNA 药剂的安全包装
“事实上,mRNA 技术只有在合适的储存解决方案下才能发挥作用。这些解决方案必须能够安全地承受递送材料(纳米脂质体)所需的低温,”肖特医药全球产品经理尼娜·克劳特沃斯特(Nina Krautwurst)解释道,“我们研发注射剂瓶、玻璃和聚合物注射器,这些产品所使用的材料互相匹配。公司积极研究包装材料之间的最佳组合,努力支持客户实现愿景。”
一些基于mRNA 的疫苗或治疗方法需要- 80°C 或更低的极端温度环境。“鉴于此,使用聚合物注射器是一个很好的解决方案,” 尼娜(Nina)说道,“玻璃材料与聚合物材料,两者的膨胀系数明显不同。 在超低温冷冻周期内,聚合物材料制成的容器能提供优异的保护。此外,容器的密封性也至关重要,在超低温冷冻周期内,容器的密封完整性也能够得到保证 。”
肖特医药正在研究能够满足这些要求的新型材料组合。公司生产的聚合物注射器由特别研发的环烯烃共聚物(COC)注塑成型,这款产品是超低温冷藏储存的不二之选。尼娜(Nina)又说:“整个注射器,包括其中的推杆上的橡胶塞,都能做到均匀变形,储存于其中的药品可以得到安全保护。聚合物注射器内壁涂有交联硅胶层,形成优质惰性材料,具有良好的药品相容性。”
癌症、疟疾和丙型肝炎的治疗方法
去年,卡塔琳·卡里科(Katalin Karikó)和德鲁·魏斯曼(Drew Weissman)因其在mRNA方面的开创性基础研究荣获诺贝尔医学奖。他们在此领域的发现已经帮助了数百万人,而这项技术还具有无限的潜能:精确靶向治疗从前无法治愈的疾病可能将永远改变未来的医疗格局。
基于mRNA的治疗方法研究已不止于针对新冠病毒(SARS-CoV-2),相关研究正走向更广阔的领域,包括细菌感染、流感、丙型肝炎、带状疱疹、艾滋病毒、疟疾和猴痘。据德国研究型制药企业协会(vfa)统计,目前正在研发或已经上市的mRNA 药物约有 125 种。
mRNA技术也为识别和消灭癌细胞带来新的希望。癌细胞因突变而产生变异蛋白质。变异蛋白质不是健康细胞,有其独一无二的标志。这表明有可能为每个癌症患者研发个性化疗法,即一种针对个体的抗癌疫苗。目前,德国拜恩泰科(BioNTech) 和美国莫德纳(Moderna) 等公司正在研发几款癌症疫苗,这些疫苗正处于不同研发阶段。
mRNA在基因治疗方面也同样拥有光明的前景。通过RNA传递信息可以修复遗传物质中的致病性变异。针对亨廷顿氏病的初步研究试验已经取得成功。
mRNA疫苗的巨大成功凸显出该技术的潜力。它的传奇故事始于两位伟大的科学家在复印机前的一次偶然相遇。而如今,这项技术已经彻底革新并形成行业规模,为改善人类健康和增进民生福祉开辟出崭新道路。