医药分析: 从可提取物和浸出物研究到机械稳定性测试
专业药物包装分析
肖特医药服务拥有40多年的药物包装分析和专业测试经验,将专业知识和最先进的分析技术相结合。 我们的测试为全球客户提供支持,符合所有现行的 EP、USP 和 JP 管制准则。
化学耐受性
肖特医药服务提供一系列筛检服务,通过专业分析评估药物与容器相互作用的风险,制定避免这种风险的策略。容器检查和筛查
在玻璃分层筛查中,首先通过肉眼和摄像头进行目视检查,确认是否有片状颗粒。 清空容器后,使用立体显微镜检查容器是否有改变的区域,以进行更深入的表面分析,确定一组检测样本中受影响程度最高的样本。
玻璃脱片确认
SEM 断面分析与电镜相结合,用于确定脱片倾向(脱片和脱片区域的早期指标)以及玻璃内表面的侵蚀程度。
药品容器相互作用
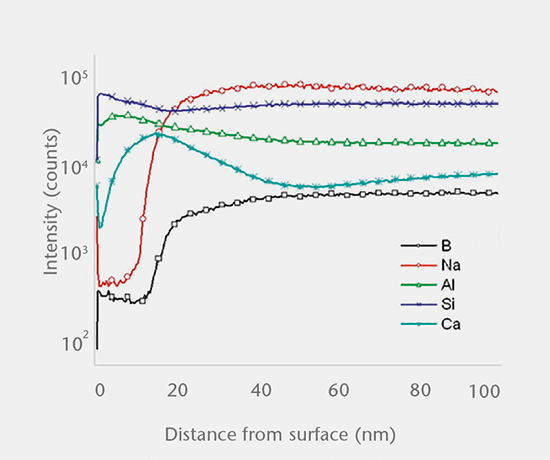
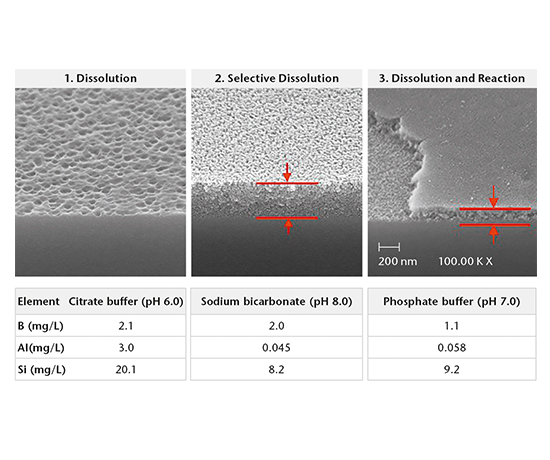
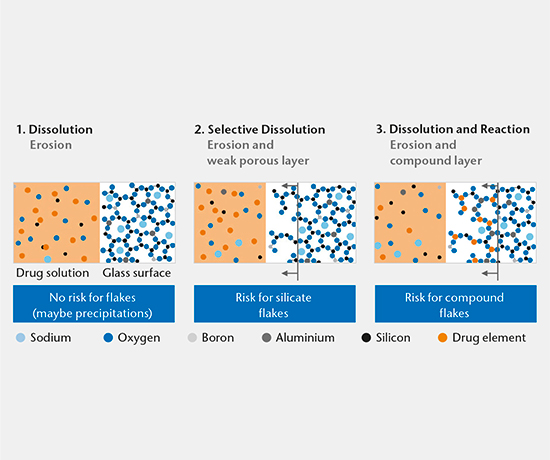
我们使用 SIMS 深度剖析、SEM 截面分析和 ICP-OES/MS 解决方案分析,来确定药品容器相互作用的机制。 主要有三种机制:
- 溶解
- 选择性溶解
- 溶解与反应
预测性实时分层研究
肖特医药服务团队根据 USP <1660> 设计了分层筛查包,用于评估产品在保存期内出现分层的可能性。 该解决方案使用一套测试方法对容器表面和近表面区域进行分析,以确定玻璃分层的风险。
颗粒分析
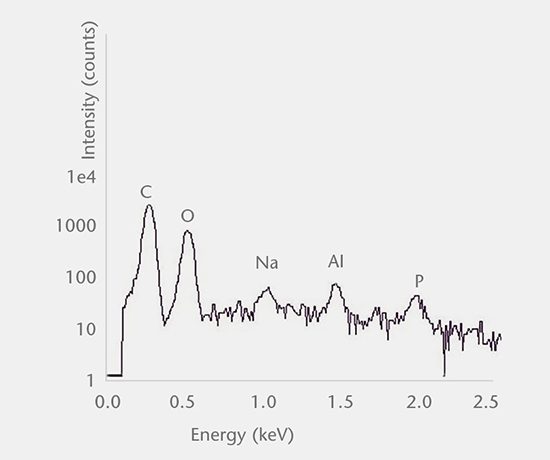
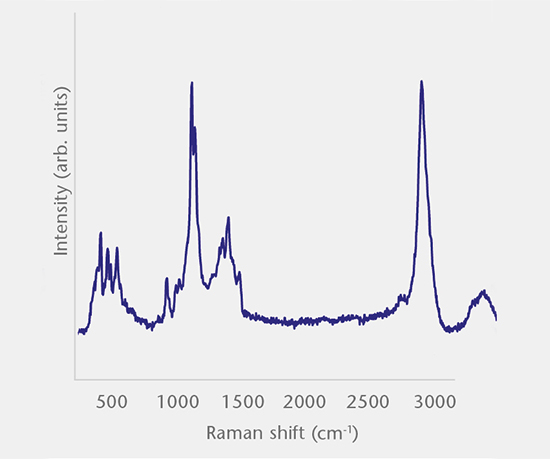
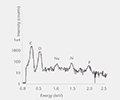
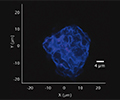
无机颗粒需要进行过滤分离,然后使用 SEM-EDS、拉曼显微镜和 FTIR 分析化学成分,并借助 SEM-EDS 进行形态分析,以确定来源。 无机颗粒的常见来源包括生产过程的副产物、加工产生的沉积物、破碎产生的颗粒以及分层产生的片状颗粒。
颗粒分析(有机)
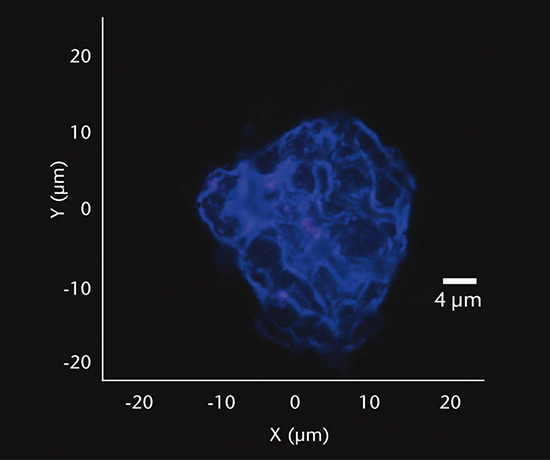
有机颗粒的评估方法与无机颗粒的分析相同。 有机颗粒的常见来源包括人源性物质(皮肤、头发)、纤维(无尘布、过滤器)和配方沉淀物或二次包装材料,如聚合物盒或收缩包装。
可提取物和浸出物/系统性能
肖特制药服务团队开发了一系列药物包装的可提取物和浸出物测试,确保满足国际管制机构的要求。可提取物和浸出物
可提取物研究
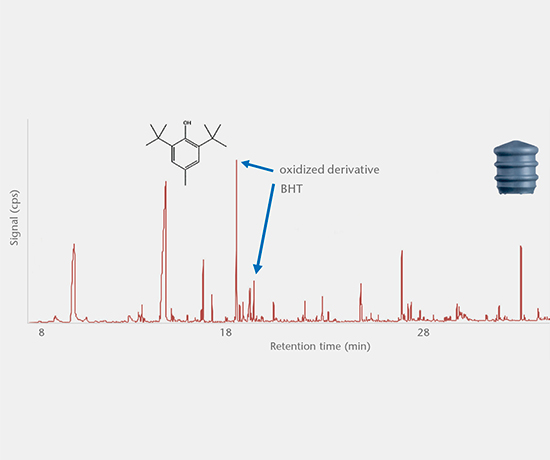
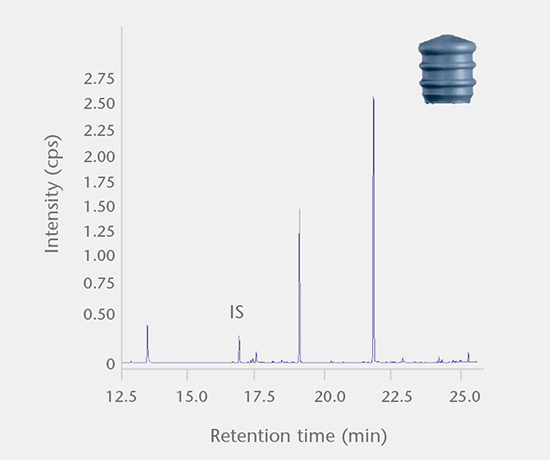
可提取物研究能够确定从初包装材料中提取的有机物质和无机物质的量,这些物质可能会迁移到药品中。 研究方案以 USP <1663>、USP <1664>、EP、ISO 10993 和 PQRI 的最新指南建议为依据。
加速实时浸出物研究
这些研究涉及方法开发和验证,然后将药品存放在密闭容器中,并在加速实时测试条件下确定药品中的浸出物和交叉反应产物。 所有分析均使用最先进的设备。 我们对 E&L 研究的支持包括对相关准则(例如 ICH M7)的专业解读,确保有效评估分析结果。 另外我们的合作伙伴还提供 E&L 数据毒理学评估的进一步支持。
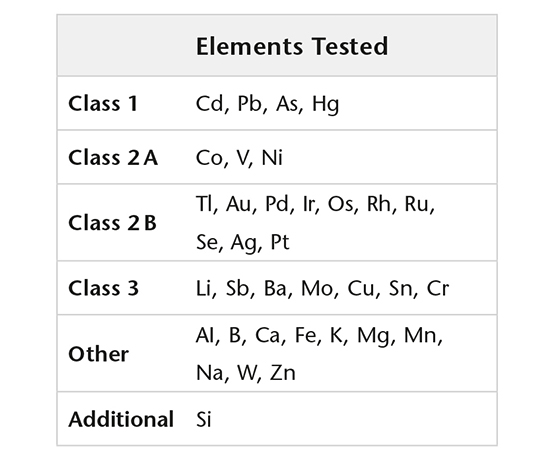
元素杂质
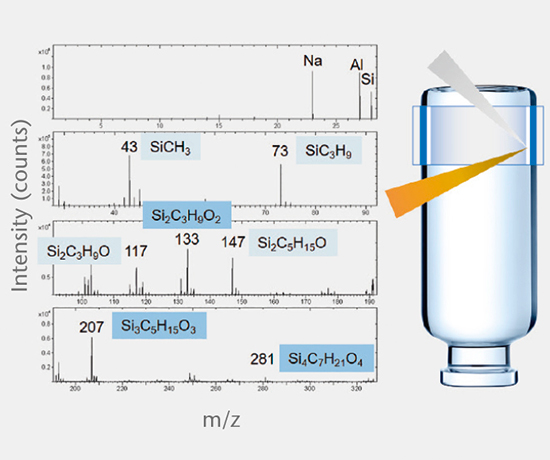
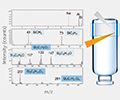
使用经过验证的方法和高分辨率 ICP-MS 测定元素杂质(USP <232>、ICH Q3D),并通过 GF-AAS 法测定可提取和可浸出的有机硅。
系统性能测试
系统性能测试
肖特医药服务团队在系统性能测试方面的专长立足于我们在玻璃、涂料、聚合物以及弹性体元件领域的长期经验和深厚功底。
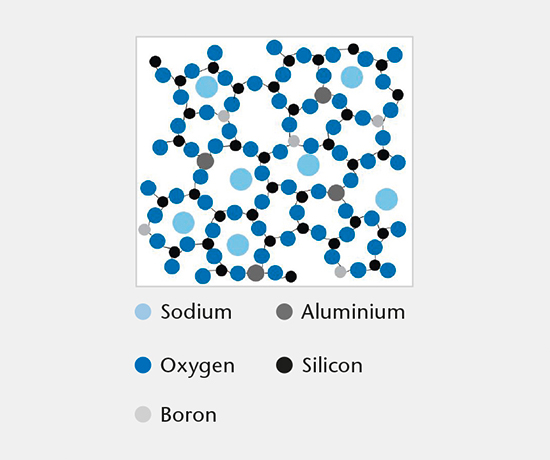
玻璃成分
该测试根据已公布的玻璃成分的综合数据库来确定初包装容器和制造商产品的玻璃化学成分。
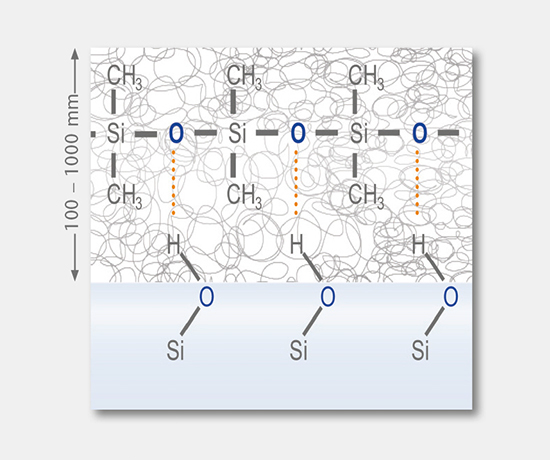
硅化、涂布和处理
这些测试涉及所用涂料和处理方法的确定,例如玻璃容器的硅油处理、阻隔涂层、疏水涂层和化学强化。
橡胶特性
我们采用多种分析方法来鉴定橡胶材料和涂层。
根据药典规定检验
肖特制药服务提供各种药物包装分析测试以及有关国际法规和标准的详细知识。 我们所有的测试方法都符合国际药典(USP/EP/JP)和行业机构( ISO、DIN、ASTM)的规定,我们可在根据药典要求进行测试的过程中提供建议和支持。
玻璃包装元件合规性
药品玻璃容器的材料合格性检验有助于制药企业确保初包装容器符合药典规定。 检验时,从批量生产中采集样本,并通过规定的方法进行检验。 玻璃容器适用的合规性检验方法包括 USP <660>、USP <211>、EP 3.2.1(碱度、耐水解性、砷),以及 ISO 9626 和 ISO 15350(注射器针头直径和成分合格性)。

弹性体密封件的合规性
药品包装弹性体密封件材料的符合性测试有助于制药企业满足药典规定。 检验时,从批量生产中采集样本,并通过规定的方法进行检验。 橡胶元件适用的合规性检验方法包括 EP 3.2.9(理化检验)和 ISO 8871(颗粒数、紫外线、灰分、密度)。
服务流程
肖特医药服务专家团队可提供一系列支持和建议,帮助您应对药品包装存在的挑战。 我们制定了完整的流程,涵盖了从初始请求到获得有效解决方案的整个过程。
您为什么应与肖特合作以生产完美的封装